- TransAeris®膈肌起搏系统获准在新冠肺炎疫情期间辅助患者脱离呼吸机,将机械通气时间缩短25%以上,从而腾出重要设备、重症监护病床和临床资源。
俄亥俄州欧柏林2020年4月15日 /美通社/ -- Synapse Biomedical, Inc. (www.synapsebiomedical.com)的TransAeris®膈肌起搏系统(DPS)已获得美国食品药品监督管理局(FDA)的紧急使用授权。在当前新冠肺炎疫情期间,某些患者脱离呼吸机后,医疗机构的医生认定存在较高的撤机失败风险。Synapse Biomedical的这款系统获准用于辅助撤机,授权有效期不超过30天。
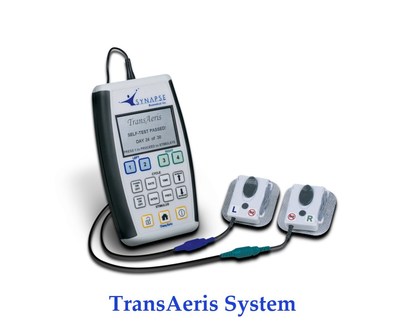
详见www.synapsebiomedical.com/covid-19
疫情期间,需要延长机械通气(PMV)的患者数量激增,对医院和重症监护病床资源的需求也空前增加。即使患者的病情已基本稳定,这些机械通气时间延长的患者仍有可能出现呼吸机引发的膈肌功能障碍(VIDD),进一步延长了机械通气时间。
TransAeris系统通过调节患者的膈肌来缓解或避免上述膈肌功能障碍的出现,从而有效解决了这一问题。这项技术近日已获得CE标志,目前正在美国进行临床研究。模型表明,该系统可以将新冠肺炎患者使用呼吸机的时间缩短26%,从而在需求巨大的特殊时期,腾出更多呼吸机。
Synapse Biomedical总裁兼首席执行官Anthony Ignagni表示:“我们的膈肌起搏技术已在全球成功治疗了2,000多名患者。非常感谢FDA的领导能向我们最新的TransAeris仪器签发紧急使用授权,这样一来,临床医生就可以在疫情期间为尽可能多的患者提供帮助。”
University Hospitals Cleveland Medical Center(克利夫兰大学医院系统医疗中心)普外科主任兼凯斯西储大学医学院(Case Western Reserve University School of Medicine)教授Raymond P. Onders(医学博士、美国外科医师协会会员(FACS))说道:“创伤以及高危外科和心脏病患者需要重症监护病床和呼吸机,而新冠肺炎患者同样也需要。在这种情况下,高危手术和新冠肺炎患者使用TransAeris后,有可能或正在延长机械通气的患者可以减少使用呼吸机的时间,有效缓解了呼吸机、重症监护病床和临床资源的供应压力。”
在TransAeris问世之前,Synapse Biomedical的另一项技术,即NeuRx®膈肌起搏系统(NeuRx DPS),自2008年以来已获得FDA认证和CE标志,成功帮助脊髓损伤(SCI)患者减少或摆脱了对机械通气的依赖。TransAeris可以为机械通气时间延长的患者提供最长30天的临时辅助治疗。此外,TransAeris简化了NeuRx DPS系统的外部设计,打造成适合患者使用的一次性器械,时间不超过30天。截止目前,欧洲的一些医疗中心,包括德国的BGU Murnau,已成功将TransAeris应用到急性脊髓损伤和多发伤患者的治疗中。

